Dengan menggunakan sebuah penelitian, kecerdasan buatan mampu mengidentifikasi kandidat antibiotik kelas baru. Senyawa ini dapat membunuh bakteri MRSA yang resisten terhadap metisilin, penyebab infeksi mematikan.
Dengan menggunakan sebuah penelitian, kecerdasan buatan mampu mengidentifikasi kandidat antibiotik kelas baru. Senyawa ini dapat membunuh bakteri MRSA yang resisten terhadap metisilin, penyebab infeksi mematikan.
D
i Amerika Serikat (AS) lebih dari 10.000 kematian setiap tahunnya oleh resistensi bakteri. Di negara ini Staphylococcus aureus (MRSA), bakteri yang resisten terhadap obat, menginfeksi lebih dari 80.000 orang setiap tahun. Bakter ini seringkali menyebabkan infeksi kulit atau pneumonia. Kasus yang parah dapat menyebabkan sepsis, infeksi aliran darah yang berpotensi fatal.
Untuk mengatasi MRSA yang resisten terhadap obat, para peneliti Massachusetts Institute of Technology (MIT) telah menemukan sekelompok senyawa yang dapat membunuh bakteri yang resisten terhadap obat. Dalam menemukan senyawa tersebut mereka menggunakan jenis kecerdasan buatan (artificial intelligence) yang mampu melakukan pembelajaran secara mendalam (deep learning).
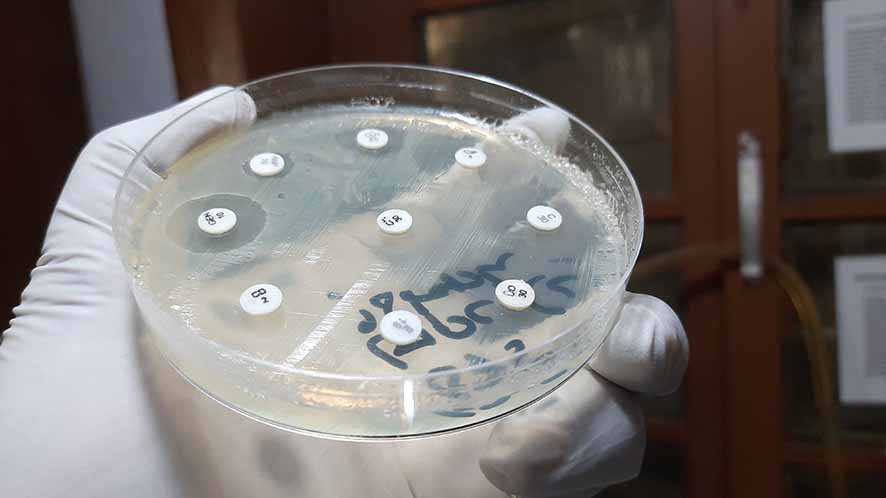
Dalam sebuah penelitian yang diterbitkan di Nature beberapa waktu lalu, para peneliti menunjukkan bahwa senyawa ini dapat membunuh MRSA. Bakteri ini termasuk dalam kelompok bakteri Staphylococcus yang jika dilihat di bawah mikroskop berbentuk bulat-bulat yang mirip seperti anggur.
Pada penelitian itu MRSA dikenal resisten terhadap metisilin ditumbuhkan di piring laboratorium selanjutnya diberikan pada dua model tikus yang terinfeksi MRSA. Senyawa ini juga menunjukkan toksisitas yang sangat rendah terhadap sel manusia, menjadikannya kandidat obat yang baik.
Inovasi utama dari studi baru ini adalah para peneliti juga dapat mengetahui jenis informasi apa yang digunakan model pembelajaran mendalam untuk membuat prediksi potensi antibiotik. Pengetahuan ini dapat membantu peneliti merancang obat tambahan yang mungkin bekerja lebih baik daripada obat yang diidentifikasi dalam model.
"Pemahamannya di sini adalah kita bisa melihat apa yang dipelajari oleh model untuk membuat prediksi bahwa molekul tertentu akan menghasilkan antibiotik yang baik. Pekerjaan kami menyediakan kerangka kerja yang hemat waktu, hemat sumber daya, dan berwawasan mekanis, dari sudut pandang struktur kimia, dengan cara yang belum pernah kami lakukan hingga saat ini," kata Profesor Teknik Medis dan Sains Termeer di Institut Teknik dan Sains Medis (IMES) MIT dan Departemen Teknik Biologi, James Collins.
Collins menuliskan penelitiannya bersama Felix Wong, seorang peneliti S-3 di IMES dan Broad Institute of MIT dan Harvard, dan Erica Zheng, mantan mahasiswa pascasarjana Harvard Medical School yang menjadi penulis utama penelitian ini.
Collins menerangkan, tim tersebut merupakan bagian dari Proyek Antibiotik-AI di MIT. Misi proyek ini, yang dipimpin oleh Collins adalah menemukan kelas antibiotik baru terhadap tujuh jenis bakteri mematikan, selama tujuh tahun.
Selama beberapa tahun terakhir, Collins dan rekan-rekannya di Klinik Abdul Latif Jameel untuk Pembelajaran Mesin di fakultas Kesehatan MIT telah mulai menggunakan pembelajaran mendalam untuk mencoba menemukan antibiotik baru. Pekerjaan mereka telah menghasilkan obat yang potensial untuk melawan Acinetobacter baumannii, bakteri yang sering ditemukan di rumah sakit, dan banyak bakteri yang resisten terhadap obat lainnya.
Senyawa tersebut diidentifikasi menggunakan model pembelajaran mendalam yang dapat belajar mengidentifikasi struktur kimia yang terkait dengan aktivitas antimikroba. Model-model ini kemudian menyaring jutaan senyawa lain, menghasilkan prediksi senyawa mana yang mungkin memiliki aktivitas antimikroba kuat.
Jenis penelusuran ini telah terbukti membuahkan hasil. Namun salah satu keterbatasan pada pendekatan ini adalah modelnya bersifat "kotak hitam", yang artinya tidak ada cara untuk mengetahui fitur apa yang menjadi dasar prediksi model tersebut. Jika para ilmuwan mengetahui bagaimana model tersebut membuat prediksi, akan lebih mudah bagi mereka untuk mengidentifikasi atau merancang antibiotik tambahan.
"Apa yang ingin kami lakukan dalam penelitian ini adalah membuka kotak hitam," kata Wong. "Model-model ini terdiri dari sejumlah besar kalkulasi yang meniru koneksi saraf, dan tidak ada yang benar-benar tahu apa yang terjadi di baliknya," kata dia dikutip laman MTI.
Pertama, para peneliti melatih model pembelajaran mendalam menggunakan kumpulan data yang diperluas secara substansial. Mereka menghasilkan data pelatihan ini dengan menguji sekitar 39.000 senyawa untuk mengetahui aktivitas antibiotik terhadap MRSA, dan kemudian memasukkan data ini, ditambah informasi tentang struktur kimia senyawa tersebut, ke dalam model.
"Pada dasarnya Anda dapat merepresentasikan molekul apapun sebagai struktur kimia, dan Anda juga dapat memberi tahu modelnya apakah struktur kimia tersebut bersifat antibakteri atau tidak," kata Wong.
"Model ini dilatih dengan banyak contoh seperti ini. Jika Anda kemudian memberinya molekul baru, susunan atom dan ikatan baru, hal ini dapat memberi tahu Anda kemungkinan bahwa senyawa tersebut diprediksi bersifat antibakteri," imbuh dia.
Adaptasi Algoritma
Untuk mengetahui bagaimana model tersebut membuat prediksinya, para peneliti mengadaptasi algoritma yang dikenal sebagai pencarian silsilah Monte Carlo. Cara ini yang telah digunakan untuk membantu membuat model pembelajaran mendalam lainnya, seperti AlphaGo, lebih mudah dijelaskan.
Algoritma pencarian ini memungkinkan model untuk menghasilkan tidak hanya perkiraan aktivitas antimikroba setiap molekul, namun juga prediksi substruktur molekul mana yang kemungkinan besar bertanggung jawab atas aktivitas tersebut.
Untuk lebih mempersempit kandidat obat, para peneliti melatih tiga model pembelajaran mendalam tambahan untuk memprediksi apakah senyawa tersebut beracun bagi tiga jenis sel manusia yang berbeda. Dengan menggabungkan informasi ini dengan prediksi aktivitas antimikroba, para peneliti menemukan senyawa yang dapat membunuh mikroba namun memiliki efek buruk yang minimal pada tubuh manusia.
Dengan menggunakan kumpulan model ini, para peneliti menyaring sekitar 12 juta senyawa, yang semuanya tersedia secara komersial. Dari koleksi ini, model mengidentifikasi senyawa dari lima kelas berbeda, berdasarkan substruktur kimia di dalam molekul, yang diperkirakan aktif melawan MRSA.
Para peneliti membeli sekitar 280 senyawa dan mengujinya terhadap MRSA yang ditanam di laboratorium. Langkah ini memungkinkan mereka mengidentifikasi dua, dari kelas yang sama, yang tampaknya merupakan kandidat antibiotik yang sangat menjanjikan.
"Dalam pengujian pada dua model tikus, satu model infeksi MRSA kulit dan satu model infeksi MRSA sistemik, masing-masing senyawa tersebut mengurangi populasi MRSA sebanyak 10 kali lipat," tulis Collins.
Percobaan mengungkapkan bahwa senyawa tersebut tampaknya membunuh bakteri dengan mengganggu kemampuan mereka untuk mempertahankan gradien elektrokimia melintasi membran sel mereka. Gradien ini diperlukan untuk banyak fungsi penting sel, termasuk kemampuan menghasilkan ATP (molekul yang digunakan sel untuk menyimpan energi).
Kandidat antibiotik yang ditemukan laboratorium Collins pada tahun 2020, halicin, tampaknya bekerja dengan mekanisme serupa tetapi spesifik untuk bakteri Gram-negatif (bakteri dengan dinding sel tipis). MRSA adalah bakteri Gram positif, dengan dinding sel lebih tebal.
"Kami memiliki bukti yang cukup kuat bahwa kelas struktural baru ini aktif melawan patogen Gram-positif dengan secara selektif menghilangkan kekuatan motif proton pada bakteri," kata Wong. hay/I-1